脊髓损伤是一种严重的中枢神经系统疾病,全球约有1500万患者,其中中国患者超过300万,每年新增病例约10万例。脊髓损伤后,患者往往出现全身或部分瘫痪,丧失运动和感觉功能,目前临床缺乏有效的神经再生修复手段,主要依靠康复训练和辅助支持治疗。
脊髓损伤难以修复的主要原因包括神经再生能力有限和损伤后微环境恶化。损伤后引发的缺血、炎症爆发、胶质瘢痕形成等一系列继发性反应,会进一步破坏剩余的神经组织,形成恶性循环。
创新疗法:iPSC衍生脊髓神经祖细胞
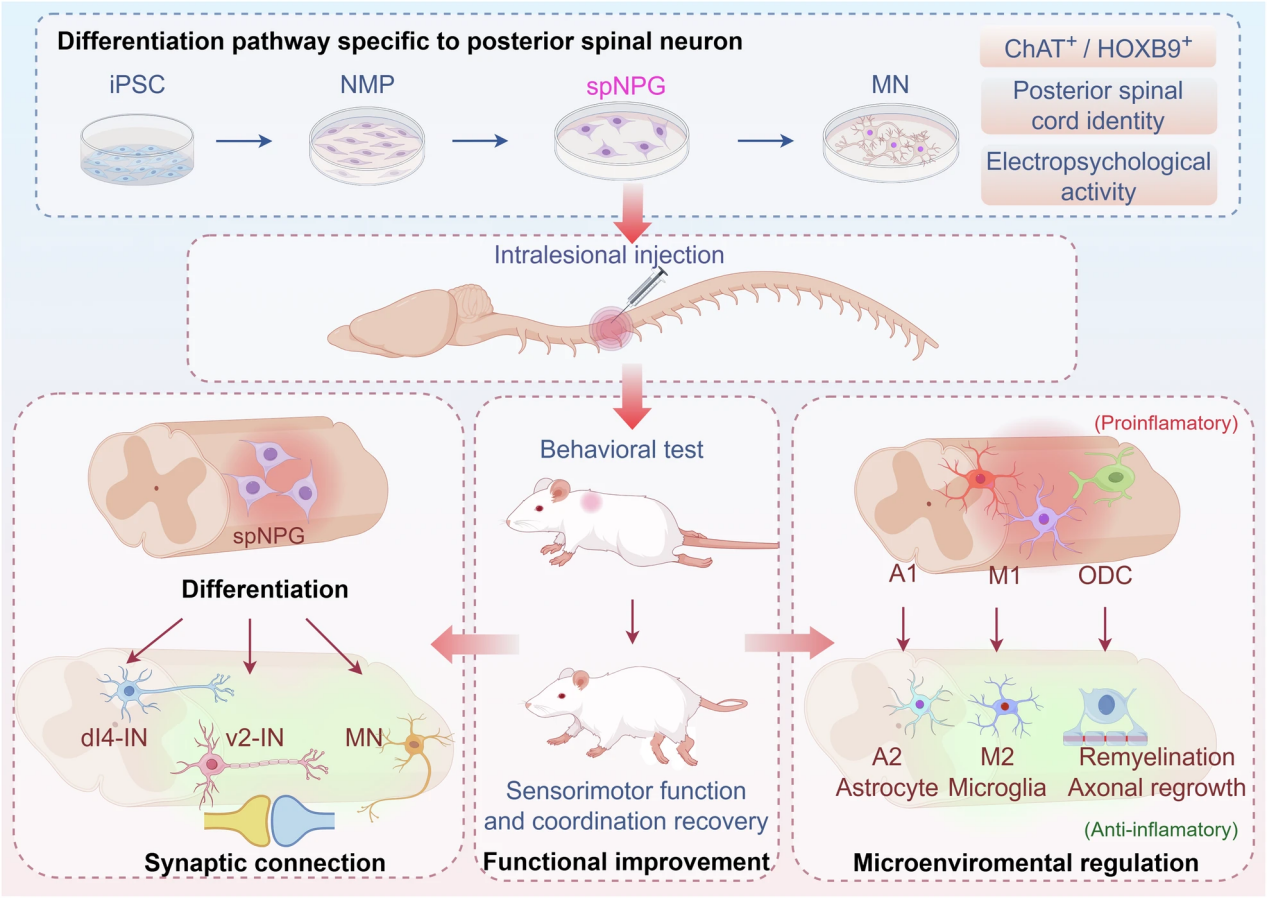
研究团队采用人诱导多能干细胞(iPSC)治疗策略,通过移植iPSC衍生的脊髓神经祖细胞(spNPG),在脊髓损伤动物模型中实现了感觉及运动功能的显著恢复。士泽生物自主研发的XS228注射液是全球首款iPSC衍生脊髓神经祖细胞治疗产品,已获得中美药监局批准开展注册临床试验。
目前,由中山大学附属第三医院牵头,联合大连医科大学附属第一医院开展的全球首个注册临床I/II期试验已完成首例受试者给药,并取得初期积极成效。
研究成果:显著的功能恢复和双重治疗机制
在动物实验中,治疗组表现出显著的运动功能改善:
Basso动物评分(BMS)达到4.5分(对照组仅为1.2分)
倾斜梯子攀爬测试正确步数是对照组的2.3倍
网格攀爬测试抓握次数是对照组的1.8倍
研究人员通过单核RNA测序等技术,揭示了spNPG的双重治疗机制:
一方面,spNPG在体内分化为运动神经元(16%)、V2中间神经元(11%)和dI4中间神经元(29.4%)等关键神经细胞,重建神经环路。这些细胞能与宿主神经细胞形成突触连接,实现信号互通。
另一方面,spNPG能调节损伤部位微环境,促进M2型小胶质细胞(抗炎型)标志物表达量升高,同时抑制A1型星形胶质细胞(促炎型)表达,减少胶质瘢痕形成,为轴突再生创造条件。
临床意义与展望
这项研究不仅为XS228注射液治疗脊髓损伤提供了强有力的临床前证据,更首次完整揭示了spNPG从体外分化到体内发挥作用的全过程,明确了"分化为神经细胞重建环路"和"调节微环境促进修复"的双重药理机制。
士泽生物自主研发的XS228注射液作为国家I类新药,已获中美药监局批准开展注册临床试验,是全球中枢神经损伤修复领域的重要里程碑。该研究对探索再生脊髓神经细胞移植治疗脊髓损伤的安全性及疗效具有重要的标杆意义,为脊髓损伤患者带来了新的治疗希望。
随着这项技术的临床转化推进,"脊髓损伤后重新行走"有望从梦想变为现实。